Троценко Татьяна Викторовна, врач-дерматовенеролог, косметолог, ведущий специалист, ООО «Астрея», Москва
Фитопрепараты по-прежнему остаются актуальными и востребованными косметическими и лекарственными средствами благодаря сочетанию эффективности, высокой биодоступности и безопасности. Тем не менее процесс экстракции биологически активных веществ из растительного сырья сопряжен с высоким риском их частичного или полного разрушения. Стандартизированные экстракты содержат фиксированную дозу активного вещества. Иллюстрацией их преимуществ можно считать результаты сравнительного лабораторного исследования антиоксидантных свойств некоторых экстрактов папоротника Polypodium leucotomos, включая стандартизированный экстракт Fernblock® (Cantabria Labs, Испания).
Казалось бы, бурное развитие производства синтетических лекарственных и косметических средств грозит вытеснить фитопрепараты и поставить под сомнение их необходимость. Тем не менее средства на растительной основе по-прежнему не теряют своей актуальности и востребованности, и вполне заслуженно. Зачастую фитопрепараты обладают клинически доказанной эффективностью, имея при этом более высокую биодоступность и переносимость в терапевтических дозах, широкий диапазон лечебных свойств и меньшее количество побочных эффектов. Для них менее характерны ограничения по продолжительности применения и возрастной группе. Однако процесс создания средств на растительной основе имеет свои подводные камни.
ПРЕМУДРОСТИ ЭКСТРАКЦИИ
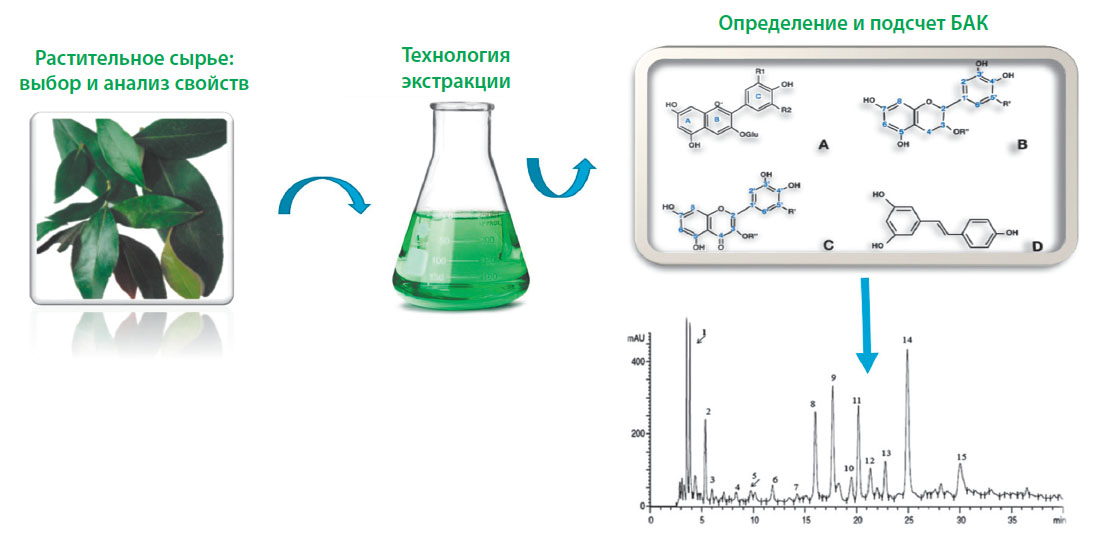
Задача с первого взгляда кажется простой: существуют растения, содержащие в себе ценные биологически активные вещества, остается только создать на их основе фитопрепарат для местного или системного применения. Процесс извлечения одного или нескольких биологически активных компонентов (БАК) из растительного сырья называется экстракцией (рис. 1). Полученный экстракт может сам по себе выступать в роли лекарственного средства или стать основой для создания комплексного препарата.
Рис. 1. Процесс экстракции биоактивных компонентов: от выбора растительного сырья до подсчета активных веществ [3]
Процесс экстракции можно разделить на несколько этапов.
1. Подготовительный этап включает сбор растительного сырья, проверку его подлинности, сортировку и очистку от примесей. Уровень концентрации действующих веществ растительного лекарственного сырья зависит от ареала произрастания, высоты местности, возраста растений, климата, типа почвы, времени сбора. Химический состав сырья также варьирует в зависимости от экологических факторов [1].
2. Уточнение природы составных частей или вторичных метаболитов, поскольку лекарственные и ядовитые свойства растений зачастую обусловлены именно этими соединениями.
3. Сушка и измельчение. Большинство химических компонентов термически нестабильны и могут подвергнуться частичной или полной деградации при нарушении температурного режима. Сушка растительного сырья проводится предпочтительно в тени при комнатной температуре или в воздушной печи при температуре не выше 30 °С. Ультрафиолетовые лучи солнечного света могут вызвать нежелательные химические реакции, поэтому по возможности нужно избегать непосредственного контакта с ними. При повышенных температурах также возможен грибковый рост, который путем ферментации и аэрации может изменить содержание и характер вторичных метаболитов. Измельчение растительного сырья позволяет увеличить площадь контакта экстрагента с растительной массой, разрушить клетки растительного сырья для высвобождения биологически активных веществ.
4. Выбор экстрагента для экстракции. В основе непосредственно экстракции лежит процесс взаимодействия растительного сырья и растворителя-экстрагента, обладающего избирательной способностью растворять только те целевые компоненты, которые необходимо выделить. Движущей силой данного процесса является разница концентраций БАК в твердом растительном сырье и растворителе, находящемся в контакте с поверхностью твердых частиц. Механизм экстракции включает в себя проникновение растворителя-экстрагента в поры твердого материала, растворение целевых компонентов, перенос экстрагируемых веществ вглубь растворителя посредством диффузии [1].
Вещества, входящие в состав лекарственных растений, принято делить на три группы:
I — действующие, или фармакологически активные соединения, которые обладают лечебными свойствами;
II — сопутствующие, которые способствуют всасыванию действующих веществ или изменяют их свойства;
III — балластные, которые не имеют фармакологического значения, однако их свойства учитываются при переработке сырья [2].
Чтобы обеспечить полноту извлечения действующих веществ и максимальную скорость экстракции, экстрагент должен обладать следующими свойствами:
– растворять максимальное количество биологически активных веществ и минимальное — балластных веществ;
– легко диффундировать через клеточную мембрану;
– быть физиологически и химически индифферентным;
– не взаимодействовать с экстрагируемыми веществами;
– препятствовать развитию микроорганизмов, грибков, плесени.
Выбор экстрагента, кроме этого, зависит от таких физико-химических свойств извлекаемого вещества, как полярность, рН, термостабильность. В качестве экстрагента могут выступать вода, глицерин, спирты, эфиры, уксусная кислота и некоторые другие вещества [3].
Для интенсификации процессов экстракции применяются такие модифицированные формы экстракции, как микроволновая экстракция, экстракция под высоким давлением, экстракция с использованием ультразвука, электроимпульсная экстракция, сверхкритическая флюидная экстракция, вакуумная экстракция и др. Полученную жидкость концентрируют выпариванием, чтобы получить жидкий экстракт, или концентрируют почти досуха, получая твердый экстракт.
ЭКСТРАКТ ЭКСТРАКТУ РОЗНЬ
Таким образом, каждый этап экстракции БАК сопряжен с существенным риском их полной или частичной потери в силу нестабильности и зависимости от внешних физических и химических факторов. Экстракты одного и того же растения могут существенно отличаться по своим биологически активным свойствам в силу как особенностей
растительного сырья (географическое происхождение, условия выращивания), так и технологии экстракции.
Стандартизированные экстракты содержат определенную фиксированную долю активного вещества. Подобного состава удается достичь благодаря химическому анализу. Высокоэффективная жидкостная хроматография, газовая хроматография, жидкостная и тонкослойная хроматография являются ключевым звеном стандартизации.
По сравнению с обычными экстрактами стандартизированные экстракты имеют ряд абсолютных преимуществ:
– гарантируют постоянное качество лекарственного средства;
– имеют более высокую концентрацию активных веществ в результате удаления балластных веществ;
– могут храниться в течение длительного периода;
– обладают более высоким уровнем биоактивности;
– легче усваиваются организмом.
Наглядной демонстрацией преимущества стандартизированных экстрактов могут стать результаты сравнительного исследования некоторых из известных коммерческих экстрактов папоротника Polypodium leucotomos (PL), включая стандартизированный экстракт Fernblock® (Cantabria Labs, Испания), проведенного учеными из Испании под руководством Сальвадора Гонсалеса (Salvador González) [4].
СОПОСТАВЛЕНИЕ РАЗЛИЧНЫХ ЭКСТРАКТОВ ЭПИФИТНОГО ПАПОРОТНИКА POLYPODIUM LEUCOTOMOS
Polypodium leucotomos (PL) представляет собой разновидность папоротников, произрастающих в тропиках и субтропиках восточной части Северной и Южной Америки. Растение использовалось в народной центральноамериканской медицине при многих болезнях (рис. 2).
Рис. 2. Папоротник Polypodium leucotomos
Благодаря высокому содержанию фенольных компонентов экстракт папоротника (PLE) обладает выраженными антиоксидантными, антимутагенными, противовоспалительными и иммуномодулирующими свойствами. В PLE содержатся:
– фенольные кислоты (феруловая, кофейная, ванильная, коричная, кумаровая, хлорогеновая, 3,4-дигидроксибензойная кислота и др);
– флавоноиды — растительные пигменты, обладающие антиоксидантными, противовоспалительными и противоопухолевыми свойствами;
– сахара (фруктоза, манноза, глюкоза) [5].
PLE начал использоваться в качестве основного или дополнительного средства лечения кожных заболеваний еще с 1970-х гг. За это время накопилось достаточно свидетельств о клинической эффективности и безопасности PLE при терапии нарушений пигментации, в составе комплексной фототерапии заболеваний кожи, при фотодерматозах, в качестве средства фотоиммунозащиты.
В подавляющем большинстве клинических испытаний использовались стандартизированные формы PLE [4].
В табл. 1 приводятся свойства PLE, позволяющие оказывать защитное действие от ультрафиолетового излучения, вмешиваясь сразу в несколько звеньев патологических изменений [6].
Таблица 1. Фотозащитные эффекты экстракта P. leucotomos [5, 6]
Материалы и методы
В исследование были включены шесть различных PLE. № 1–3 — экстракты листьев и № 4–6 — экстракты
корневища:
• № 1 — буферный водный раствор PLE при нейтральном рН;
• № 2 (Fernblock®) — водный PLE при щелочном рН;
• № 3 — водно-спиртовой PLE при кислом рН;
• № 4 — гранулированный водно-спиртовой PLE;
• № 5 — водно-спиртовой PLE;
• № 6 — водно-гликолевый PLE.
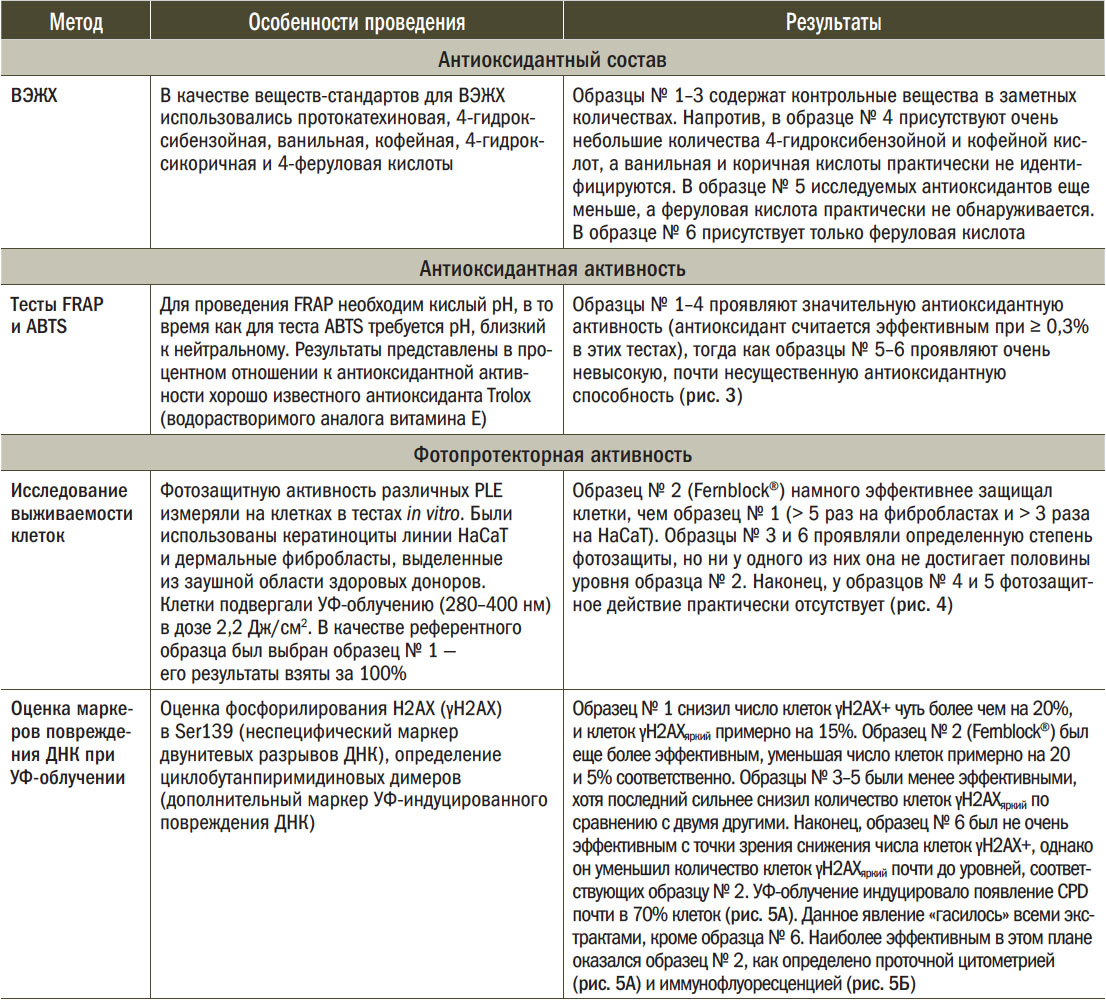
С целью определения содержания в экстрактах антиоксидантов был использован метод высокоэффективной жидкостной хроматографии (ВЭЖХ), для оценки биологической активности — неклеточные и клеточные модели (табл. 2).
Таблица 2. Результаты сопоставления состава и антиоксидантных свойств различных PLE [4]
Результаты
Метод ВЭЖХ показал различия в составе и количественном содержании ароматических кислот, об-ладающих антиоксидантными свойствами. Три экстракта, изготовленные из листьев PL, оказались более насыщенными ароматическими кислотами-антиоксидантами по сравнению с экстрактами корневищ.
В большей степени это касается 3,4-дигидроксибен-зойной и 4-гидроксибензойной кислот, которые отсутствуют в двух экстрактах корневищ и присутствуют в очень небольшом количестве в третьем (образец № 4). Что касается экстрактов листьев, наиболее очевидным их отличием является значительное
присутствие 3,4-дигидроксибензойной и 4-гидроксибензойной кислот, а также 4-гидроксикоричной кислоты. Совместное действие этих трех антиоксидантов может лежать в основе выраженных фотопротекторных свойств экстрактов листьев. Вместе с тем нельзя исключать вклад дополнительных веществ, относящихся к разным химическим группам (пептиды, ароматические соединения и пр.).
Наблюдалась прямая зависимость между выживаемостью клеток и уровнем маркеров повреждения ДНК.
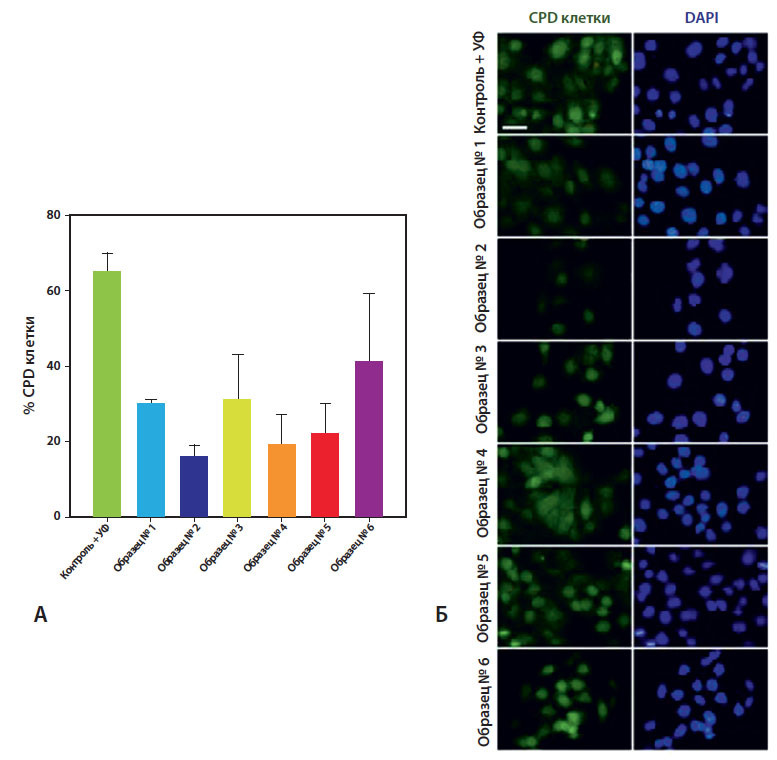
Действительно, референтный экстракт (образец № 2, Fernblock®) проявил себя самым эффективным фотопротектором по всем показателям, используемым в данном исследовании: выживаемость клеток, фосфорилирование H2AX и появление циклобутанпиримидиновых димеров (CPD). Остальные экстракты проявляли смешанную эффективность (см. табл. 2).
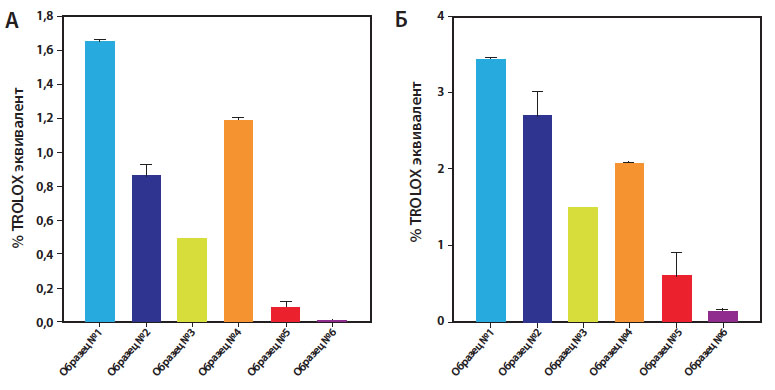
Рис. 3. Определение антиоксидантов в неклеточной системе при помощи анализа FRAP (A) и ABTS (Б) [4]
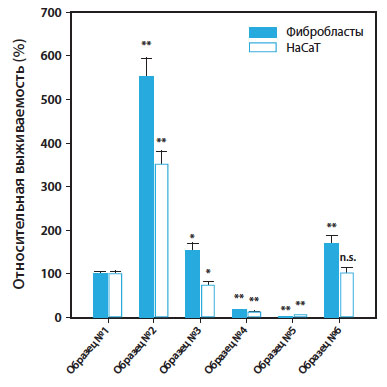
Рис. 4. Влияние на выживаемость клеток различных экстрактов P. leucotomos [4]
Рис. 5. Влияние различных экстрактов на появление циклобутанпиримидиновых димеров (CPD) [4] А — проточная цитометрия, Б — иммунофлуоресцентный анализ (пояснения
в тексте)
Выводы
Исследуемые PLE отличались между собой по содержанию веществ-антиоксидантов, антиоксидантной активности и выраженности фотозащитных свойств. Подобная вариабельность свойств экстрактов одного и того же растения может быть обусловлена используемой частью растения, методом экстракции и, возможно, географическим происхождением и условиями роста, временем и методом сбора урожая, процессом высушивания и измельчения, условием хранения сырья. Стандартизированный экстракт Fernblock® (образец № 2) характеризовался наиболее выраженными антиоксидантными свойствами и фотопротекторной активностью.
FERNBLOCK® — СТАНДАРТИЗИРОВАННЫЙ PLE
Существует большое количество публикаций, посвященных исследованию состава, механизма действия и опыту клинического применения PLE. Однако все эти исследования относятся исключительно к одной формуляции PLE, известной как Fernblock® — стандартизированный концентрированный водорастворимый экстракт листьев папоротника PL.
Разработка препарата велась испанским концерном IFC Group (в настоящее время — Cantabria Labs) совместно с Гарвардской медицинской школой и ведущими международными экспертами в области дерматологии и фотозащиты, в том числе Томасом Фицпатриком.
Производство Fernblock® и пищевых добавок с его содержанием сертифицирована по стандарту GMP (Надлежащая производственная практика) и FDA (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США).
Качество препарата является следствием кропотливой работы и строгого контроля на каждой стадии. Природосберегающее производство Fernblock® находится в Центральной Америке (Гондурас) (рис. 6).
Рис. 6. Контролируемые условия выращивания Polypodium leucotomos для изготовления экстракта Fernblock®
Выбор источника сырья:
– контролируемые условия выращивания (состав почвы, освещение, вентиляция, температура, высота над уровнем моря, полив, обработка удобрениями, густота посадки);
– для производства экстракта используются листья, в которых благодаря контакту с солнцем (фотосинтез, защита от радиации) в наибольшей концентрации содержатся энзимы, по мере созревания листья срезаются вручную, а затем высушиваются и перемалываются в строго установленных, контролируемых условиях;
– анализ на присутствие пепла, влажности, тяжелых металлов, микробных загрязнений, альфатоксинов, пестицидов и гербицидов;
– хранение в строго установленных, контролируемых условиях во избежание порчи на пути в Испанию.
Получение экстракта:
– водная экстракция (более безопасная и экологичная, позволяет осуществить более тщательную, прицельную экстракцию; алкогольная экстракция менее дифференцированна, в экстракт попадает больше субстанций, в т.ч. инертных, не имеющих никакого действия);
– контроль температуры и продолжительности процесса;
– аналитический контроль (присутствие активных ингредиентов на установленном уровне и отсутствие
примесей) и контроль эффективности (фотозащита, антиоксидантное действие).
Анализ и оценка состава, свойств и токсичности экстракта Fernblock® проводятся для каждой партии продуктов, чтобы обеспечить стандарт качества.
В 2015 г. был проведен комплексный тест на токсикологическую безопасность и соответствие международным стандартам, в ходе которого продемонстрирована полная переносимость экстракта PLE. Результаты метаанализа клинических и доклинических исследований применения PLE за 40-летний период свидетельствуют о высоком профиле безопасности: PLE назначался внутрь в дозе от 120 до 1080 мг, только у 2% пациентов отмечались нежелательные явления в виде зуда или нарушения работы желудочно-кишечного тракта. Исследования продолжительного применения препарата на протяжении 90 и 60 дней также подтверждают безопасность PLE и его эффективность в устранении деструктивных эффектов УФ.
Технология Fernblock® легла в основу создания средств линии Heliocare, обеспечивающих топическую и пероральную фотозащиту.
СРЕДСТВА ФОТОИММУНОЗАЩИТЫ HELIOCARE
В привычном понимании защита от деструктивного действия солнечного излучения заключается в нанесении местных солнцезащитных средств. При этом недостаточно учитываются некоторые немаловажные факты:
– потеря эффективности из-за контакта с водой, песком, потом;
– некорректное использование топических фотозащитных средств (позднее или недостаточное нанесение);
– наличие незащищенных частей тела (уши, веки и др.);
– нестабильность фильтров.
Таким образом, пероральные фотозащитные средства Heliocare® на основе Fernblock® позволяют усилить
собственную фотоиммунную защиту кожи, что особенно актуально для пациентов группы риска (светлые фототипы кожи, пациенты с гиперпигментацией, высокий риск злокачественных заболеваний кожи), а также при нарушении правил использования топических средств защиты (табл. 3).
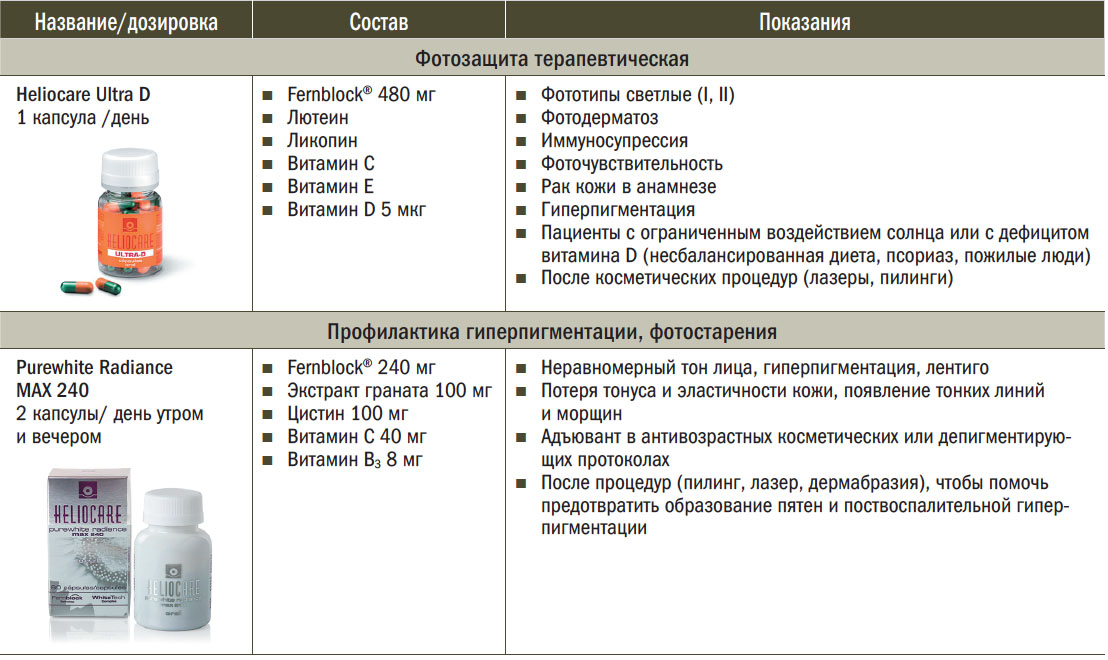
Таблица 3. Линия пероральных средств фотоиммунной защиты Heliocare®
Топические средства Heliocare® обладают фотозащитными свойствами с широким спектром покрытия благодаря комбинации химических и физических фильтров, оберегающих от УФ-А/В-излучения, и Fernblock® — специального фотопротекторного щита от инфракрасного и видимого излучения (табл. 4). Технология Sunsphere® повышает эффективность фильтров и позволяет использовать их в более низких количествах, что снижает потенциальный риск раздражения или аллергии.
Таблица 4. Топические средства Heliocare®
ЗАКЛЮЧЕНИЕ
Средства на основе стандартизированных экстрактов представляют собой препараты с точным содержанием БАК, прогнозируемым клиническим эффектом и высоким профилем безопасности. Это существенно расширяет границы их применения и повышает доверие к фитотерапии со стороны пациентов. Результаты лабораторных и клинических исследований стандартизированного экстракта Fernblock® и средств на его основе являются яркой иллюстрацией реализации целебных свойств растений посредством современных технологий в высокоэффективный, безопасный и удобный в применении препарат.